Dra. Dianora Navarro Gastroenterólogo pediatra. Coordinador de Postgrado. Unidad de Gastroenterología y Nutrición Pediátrica. Hospital Dr. Miguel Pérez Carreño. IVSS, Caracas-Venezuela.
RESUMEN
La enfermedad celiaca (EC) es una condición autoinmune con base genética, ya que se desarrolla en personas susceptible en respuesta a la exposición del gluten. La prevalencia mundial se estima de 1 persona por cada 100, que puede variar según la zona geográfica. Se presenta con manifestaciones intestinales y extraintestinales, que no son específicas y requiere un alto grado de sospecha. Además, puede estar asociada a otras enfermedades autoinmune. Los síntomas clásicos se deben a la malabsorción intestinal, con buena respuesta a la dieta libre de gluten. El espectro clínico extradigestivo es muy amplio con afección hematológica, neurológica, dermatológica, oral, dentaria, hepática entre otras. Se debe conocer que Diabetes mellitus tipo 1 y Tiroiditis autoinmune son patologías asociadas, donde el diagnóstico es crucial.
Palabras claves: enfermedad celiaca, dieta libre de gluten, diabetes mellitus, tiroiditis, hepatitis autoinmune, anemia.
ABSTRACT
Celiac disease (CD) is a genetically based autoimmune condition, as it develops in susceptible people in response to gluten exposure. The global prevalence is estimated at 1 person per 100, which may vary depending on the geographic area. It presents with intestinal and extraintestinal manifestations, which are not specific and requires a high degree of suspicion. In addition, it may be associated with other autoimmune diseases. The classic symptoms are due to intestinal malabsorption, with a good response to a gluten-free diet. The extra-digestive clinical spectrum is very broad with hematological, neurological, dermatological, oral, dental, liver, among others. It should be known that Diabetes mellitus type 1 and autoimmune thyroiditis are associated pathologies, where the diagnosis is crucial.
Key words: celiac disease, gluten-free diet, diabetes mellitus, thyroiditis, autoimmune hepatitis, anemia.Autor de correspondencia: Dianora Navarro, Gastroenterólogo pediatra. Coordinador de Postgrado. Unidad de Gastroenterología y Nutrición Pediátrica. Hospital Dr. Miguel Pérez Carreño. IVSS, Caracas-Venezuela, correo electrónico: dianora.navarro@hotmail.com
INTRODUCCIÓN
Enfermedad celíaca (EC) es un proceso sistémico inmunomediado provocado por el consumo de gluten y prolaminas relacionadas, en personas genéticamente susceptibles (haplotipo HLA-DQ2 / DQ8), esta condición puede presentarse con o sin enteropatía. (1) Factores que son necesarios, pero no suficientes, para desarrollar la EC.
Se estima una la prevalencia en la población general del 1% a nivel mundial. Los estudios de seroprevalencia o por biopsia comprobada se han estimado en 1,4 % y 0,7 %, respectivamente. (2-3)
La EC presenta una sintomatología variable y amplia con afectación digestiva y extradigestiva, siendo necesario el uso de marcadores serológicos y estudio histológico de la mucosa intestinal para su diagnóstico definitivo. La identificación de biomarcadores como anticuerpos contra el endomisio (EmA) y contra la transglutaminasa anti-TG2, han cambiado la epidemiología de la EC, aunque la mayoría de los pacientes con siguen sin ser diagnosticados, lo que deja el “iceberg” celíaco todavía sumergido debajo del agua. (4)
MANIFESTACIONES CLINICAS.
La clínica no es patognómica diferentes grados de severidad y en ocasiones es inespecífica o asintomáticos por lo que requiere un alto índice de sospecha. Aunque, en la última década existe una mayor consciencia y conocimiento de la EC, epidemiológicamente se estima que hasta un 95% de los pacientes celíacos aún permanecen sin diagnosticar y el retraso en el diagnóstico de la enfermedad celíaca es de 4 a 10 años. En pocos pacientes los signos clínicos son significativos de la enfermedad y la mayoría refiere síntomas no clásicos o vagos, por lo que no se puede realizar el diagnóstico o el diagnóstico se retrasa. (5)
También los síntomas pueden variar de acuerdo con la edad, en niños pequeños lo más frecuente son síntomas de malabsorción intestinal, en niños grandes, adolescentes y adultos presentan síntomas no malabsortivos. En estos grupos existe una prevalencia mayor de alteraciones ginecológicas, retraso de crecimiento y de la pubertad, osteoporosis y riesgo aumentado de fractura, así como un aumento del riesgo de malignidad intestinal en pacientes no tratados. (1,6)
El artículo de Popp y Makki (7) considerando la historia natural del desarrollo de la EC, evaluando la morfología de la mucosa intestinal normal, altura de las vellosidades y una relación de profundidad de las criptas, señalan que, tras la ingestión de gluten, la lesión de la mucosa avanza rápida o gradualmente a diferentes edades, bien sea en la niñez o solo en una edad avanzada, debido a que la tolerancia al gluten es individual y puede romperse en cualquier momento. Por ello la variedad de sintomatología a diferentes edades.
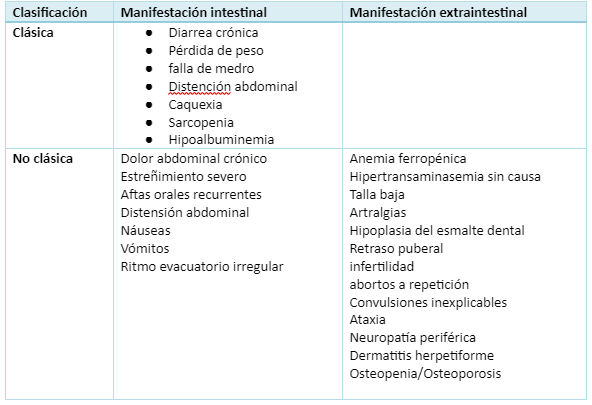
En este artículo, se tomará la descripción clínica dependiendo si involucra el tracto gastrointestinal o si los signos son extradigestivos, tabla 1, donde además se muestra la relación con las características de síntomas clásicos y no clásicos.
Manifestaciones clínicas intestinales
La forma intestinal o síntomas de malabsorción intestinal se observan con mayor frecuencia en niños, especialmente en los menores de 3 años. Se caracteriza por una diarrea crónica acompañada de distensión abdominal y pérdida de peso. Es muy frecuente que se observe retraso del crecimiento con atrofia muscular y cambio de humor como irritabilidad. (4,8-9)
El daño inflamatorio de la mucosa del intestino delgado conduce a un aumento de solutos no absorbidos en la luz con arrastre de agua, por eso la diarrea es de tipo osmótica, heces voluminosas, mal olientes y con esteatorrea. Si la lesión avanza con diferentes grados de atrofia de las vellosidades e hiperplasia de la cripta además de macronutrientes no absorbidos también se presentará el déficit micronutrientes como vitamina B12, vitaminas liposolubles, ácido fólico y el hierro. (11-12) Secundariamente la inflamación condiciona distensión abdominal y pérdida de peso.
Los niños mayores tienen menos diarrea, se manifiestan clínicamente como estreñimiento, dolor abdominal o pérdida de peso. En forma similar, los adultos presentan otros síntomas como caquexia, sarcopenia, hipoalbuminemia y trastornos hidroelectrolíticos, y la diarrea es infrecuente. (9-10,13) En ocasiones simula un Síndrome de intestino irritable, dispepsia, náusea o vómitos. (10)
Manifestaciones extraintestinales.
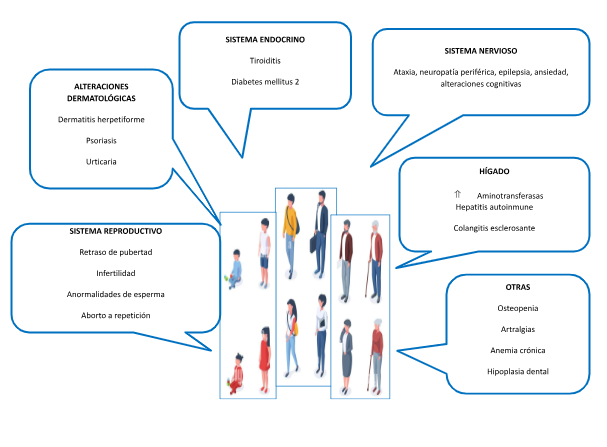
Una variedad extensa de síntomas domina las manifestaciones extraintestinales. Se detallarán de acuerdo con el órgano o sistema afectado. Los síntomas extraintestinales son comunes tanto en niños como en adultos, figura 1.
Alteraciones bucales.
Las aftas orales se observan entre el 30 a 40% de los pacientes, se caracteriza por pequeñas úlceras dolorosas bien circunscritas en la cavidad bucal. Se piensa que esta condición puede ser resultado del efecto inmunológicos directos de la exposición al gluten, ya que la dieta sin gluten (DLG) puede conducir a la remisión completa de la estomatitis y la exposición al gluten induce la recurrencia. Sin embargo, no está claro si más bien se debe a deficiencias nutricionales, como hierro, ácido fólico y vitamina B12. (4,9,14)
Los diagnósticos diferenciales incluyen Síndrome de Behcet, Enfermedad inflamatoria intestinal, Síndrome de Sweet, neutropenia cíclica e infección por VIH. (9)
Alteraciones dentarias.
Las alteraciones en el esmalte son más frecuentes en incisivos permanentes. Estos defectos del esmalte incluyen cambios de color, picaduras, surcos y pérdida completa del esmalte. También se han encontrado defectos en el esmalte dental entre familiares sanos de primer grado de pacientes con EC que portan HLA DQ2 con histología duodenal normal. (9)
Estas alteraciones en la amelogénesis de los dientes permanentes son un hallazgo bien definido en la enfermedad celíaca. Se han sugerido que la desnutrición, la hipocalcemia y los trastornos inmunológicos son factores causantes de los defectos del esmalte y la gravedad parece estar asociada con la duración de la exposición al gluten. (15) Se menciona que el defecto en el esmalte dental ocurre cuando la EC afecta a niños durante el desarrollo dental, antes de los 7 años. Cuando el defecto afecta a los dientes permanentes, no hay mejoría con la DLG. (16)
Alteraciones hematológicas.
Lo más frecuentes de la anemia microcítica por deficiencia de hierro, la cual se detecta hasta en un 40% de los pacientes, es secundaria a la malabsorción intestinal del hierro y como dato importante la anemia es refractaria al tratamiento en los pacientes sin dieta, lo cual es una recomendación para solicitar la serología. (10) Con menos frecuencia, pero no menos importante es la anemia macrocítica por deficiencia de folato o vitamina B12 (9-10) debido a la inflamación sistémica representan más del 15% de la anemia en la EC.
La anemia por deficiencia de hierro mejora con la suplementación con hierro en una dieta sin gluten, la falta de mejoría requiere más investigación. (9)
Una manifestación poco conocida es el hipoesplenismo, pudiendo estar asociada a la respuesta inmune, así como a otras manifestaciones autoinmune. Los signos clínicos de hipoesplenismo incluyen trombocitosis y cuerpos de Howell-Jolly en el frotis de sangre. (17) La importancia se centra en que causa susceptibilidad a las infecciones neumocócicas u otros gérmenes encapsulados como H. influenza por lo que requerirán vacunas estos pacientes. Adicionalmente se debe vigilar el estado de respuesta a la vacuna contra el virus de la hepatitis B, ya que se ha observado una respuesta atenuada a la vacuna entre personas con EC. (9,17).
Alteraciones hepáticas
Lo usual es una persona con ascenso de las aminotransferasas sin causa aparente. Esta elevación asintomática de menos de cinco veces el límite superior normal y con una relación AST/ALT menor a 1, en un paciente con examen normal y una ecografía hepática sin alteraciones. (10) Una prevalencia del 4% al 9% es reportada en estudios recientes (10,14). Sin embargo, otro reporte refiere que se presenta en un 40 a 50% de los no tratados. (10)
Generalmente la lesión hepática es leve y fácilmente reversible, y es lo que se denomina hepatitis idiopática o celíaca, la respuesta de la hipertransaminasemia a una DLG estricta es excelente, con una tasa de normalización completa de las enzimas hepáticas del 75 al 95% en 12 a 24 meses. (16)
De manera diferente, y en raras ocasiones la enfermedad hepática progresa a insuficiencia hepática o cirrosis, (14) como parte del mecanismo autoinmune, que no responde a la DLG. Se presentan otras patologías asociadas como Colangitis biliar primaria, Colangitis esclerosante primaria, Hígado graso asociado al metabolismo (MAFLD). (9,16) Estas formas clínicas asociada a la EC son más frecuente en adolescentes y mujeres. (9) Con respecto a la MAFLD existen una nueva redefinición en hígado graso, la investigación apunta a una afectación metabólica asociada a la dieta sin gluten, el término que puede ser empleado en niños y adultos, el diagnóstico de la EC y después de 2 años de una dieta sin gluten. (15)
La afectación hepática se puede atribuir a la translocación de antígenos bacterianos y alimentarios que llegan al hígado debido al aumento de la permeabilidad intestinal. (10,14) También se señala que la inflamación intestinal activa y la reacción inmune al gluten y la transglutaminasa tisular pueden tener efectos directos en el hígado. (9) Además, algunos estudios han informado evidencia histológica de depósitos de autoanticuerpos tTG2 en biopsias hepáticas de pacientes con EC, lo que sugiere su participación directa en el daño hepatocelular. (14,18)
Alteraciones dermatológicas.
La dermatitis herpetiforme (DH) es una manifestación extraintestinal muy frecuente, de predominio en varones. Se caracteriza por vesículas y pápulas con prurito, principalmente en la superficie extensora de miembros codos, rodillas y glúteos, aunque también en abdomen, parte superior de la espalda, el cuero cabelludo y la cara, mientras que es raro en pies y manos. (14,19) Los síntomas gastrointestinales evidentes son raros. Sin embargo, en la biopsia duodenal se describen diferentes grados de atrofia vellositaria de leve a moderada hasta un 75% de pacientes con DH con diversos, y en el resto de las personas se observan cambios inflamatorios denominados enteritis linfocítica en ausencia de atrofia vellosa. (14,18-19)
El diagnóstico de confirmación se realiza con una biopsia de piel, donde se detecta por inmunofluorescencia, depósitos de inmunocomplejos tTG3-IgA en la dermis. (14,18) Una hipótesis válida para la patogénesis inmunológica de la DH es que comienza a partir de una EC latente o manifestada en el intestino y evoluciona hacia un depósito de complejos inmunitarios de anticuerpos transglutaminasa epidérmica IgA (TG3) de alta avidez, junto con la enzima TG3, en la dermis papilar. Un grupo de pacientes responde bien a la dieta sin gluten, pero a algunos que ameritan tratmiento con dapsona (4,4-diaminodifenilsulfona), durante un promedio de 2 años. (9,14,18)
Existen otras afecciones cutáneas menos conocidas, se ha propuesto una clasificación de las enfermedades de la piel asociadas con la EC, dividiéndolas en cuatro categorías: autoinmunes (psoriasis, alopecia, vitíligo, lupus eritematoso sistémico), alérgicas (urticaria crónica, dermatitis atópica), inflamatorias (eritema migratorio microlítico, pitiriasis liquenoide, eritema nudoso) y misceláneas (estomatitis aftosa, rosácea). (19)
Alteraciones neurológicas.
El síntoma más habitual de manifestación neurológica en los pacientes es la cefalea, observada hasta en un 20%. La cefalea idiopática, la migraña y la cefalea tensional son más frecuentes entre los individuos con EC. (9) En niños pequeños es característico la irritabilidad y cambios de humor. Raramente, se observan ataxia y neuropatía en niños, estimada en 0,1% -7,4%. (16)
Se informa que la prevalencia de epilepsia en niños en 1,4 veces mayor en niños con enfermedad celíaca en comparación con la población general, aunque la relación entre la epilepsia y la EC aún no está clara. (5,16) Las convulsiones son de tipo parcial compleja, y en segundo lugar las convulsiones tónico-clónicas. Acompañada de calcificaciones cerebrales occipitales. Algunos autores consideran que se trata de un síndrome específico y diferente de la EC llamado Síndrome de Gobbi y otros autores creen que la asociación de epilepsia y calcificaciones occipitales sin lesión intestinal es una forma silenciosa o potencial de EC basándose en que tanto la epilepsia-calcificaciones cerebrales asociadas con personas HLA-DQ2 y DQ8. (20)
La ataxia por gluten en adultos es frecuente, generalmente varones y mayores de 50 años. Sin embargo, puede aparecer a cualquier edad. Representa el 40% de las ataxias de origen desconocido y el 15% de todas las ataxias. El cuadro clínico implica la participación cerebelosa de los cordones posteriores tanto de la columna como de los nervios periféricos, provocando problemas de equilibrio, marcha, inestabilidad, temblores de extremidades y nistagmo, que impiden al paciente llevar una vida normal. (9,20) Se ha reportado la presencia de autoanticuerpos transglutaminasa 6 (TG6) dependientes del gluten dirigidos contra las células cerebelosas pueden desempeñar un papel y podrían ser útiles en el diagnóstico de esta afección. Aunque en niños celiacos se ha detectado TG6 sin síntomas neurológicos. (9)
La neuropatía periférica es otra manifestación que se observa hasta en el 39% de los pacientes, precede las manifestaciones intestinales. (14) Otra sintomatología en adultos es la llamada Niebla mental, y se trata de síntomas cognitivos leves, dificultades de concentración y déficits de memoria episódica, que generalmente mejoran cuando se inicia una dieta sin gluten y reaparecen con la contaminación dietética con dieta sin gluten. (21). Se añade los trastornos psiquiátricos muy frecuentes en adultos. Cabe señalar que se han asociado a la EC ansiedad, depresión, déficit de atención o trastornos alimentarios, pero no son manifestaciones específicas. (9)
Talla baja.
Una manifestación común en niños y adolescentes es la talla baja o baja estatura puede ser una presentación inicial aislada. entre el 10 y el 40% tendrán baja estatura en el momento del diagnóstico. En los niños pequeños con sintomatología clínica grave, diarrea y desnutrición puede observarse con frecuencia un retraso grave en el crecimiento. No obstante, en la EC se estima que hasta un 10% de los niños sometidos a una evaluación de baja estatura no tienen enfermedad endocrinológica. (22)
Recientemente, un metaanálisis encontró que 1 de cada 14 pacientes con estatura baja por EC por todas las causas y uno de cada nueve pacientes con estatura baja idiopática tenían una EC confirmada por biopsia. Dichos niños responden bien y muestran un crecimiento de recuperación de la DLG si el diagnóstico se ha realizado mucho antes de la pubertad, suelen recuperar el crecimiento (> 1 SD). Si no mejora, investigar hormona del crecimiento (anticuerpos antipituitarios). (16)
El mecanismo es multifactorial, puede ser secundario a malabsorción pero otra explicación es la disfunción del eje hormona del crecimiento (GH)-factor de crecimiento similar a la insulina (IGF1) y, en particular, el papel de la grelina con valores reducidos, así como un probable mecanismo autoinmune. (16,22)
Alteraciones en el sistema reproductor.
Existe una variedad de sintomatología en relación con los órganos reproductores. La amenorrea, pubertad retrasada, menopausia precoz, infertilidad. Así como eventos obstétricos como el abortos recurrentes y retraso crecimiento fetal en asociación con EC.
Se sabe que la EC puede provocar inflamación y malabsorción. (16) El retraso de la menarquia en EC es de aproximadamente 2 años, entre las niñas que no reciben tratamiento y la amenorrea es una complicación frecuente en las niñas no tratadas, al igual que la menopáusica comienza antes del tiempo en las mujeres con EC no tratadas. (9) Según el mecanismo propuesta se señala hipopituitarismo funcional asociado con la desnutrición, que reduce las gonadotropinas y las hormonas sexuales, donde los péptidos del gluten circulantes también pueden tener un efecto inmunológico directo sobre el eje hipotálamo-pituitario-gonadal. (9,18) La dieta sin gluten puede corregir estos efectos. (9,14,16)
Enfermedades asociadas
En la EC se presenta la afectación de glándulas endocrinas como la tiroides y páncreas.
La Diabetes mellitus tipo 1 (DM1) y tiroiditis autoinmune (TA) son las más frecuentes.
La diabetes mellitus tipo 1 (DM1) se presenta más en niños o adolescentes y la tiroiditis autoinmune (TA) en adultos. El proceso fisiopatológico común, basado en una respuesta autoinmune, hace que la asociación de DM1 y AT con EC sea bastante fácil para los médicos, que a menudo solicitan un estudio serológico celíaco en este subgrupo de pacientes. (14)
La DM1, es común en EC, comparten factores genéticos y mecanismos patogénicos HLA-DQ2 está presente en el 50% de los pacientes diabéticos, pero hasta el HLA-DQ8 se detecta en aproximadamente el 70% de los pacientes con DM1. (5) Siendo la prevalencia de DM1 seis veces mayor que en EC que en la población general, los pacientes con DM1 tienen una prevalencia de EC entre 3-6% y los pacientes celíacos tienen anticuerpos contra los islotes de Langerhans, en el 4,5-11%. (23) Se ha recomendado que las pruebas de detección de EC se realicen en el momento del diagnóstico de DM1 y luego cada 2 años. (5)
Hay evidencia de que las enfermedades tiroideas autoinmunes están asociadas con la EC con una prevalencia del 3,0% al 4,8% (5) Se ha encontrado que los pacientes con TA la prevalencia de EC en 3-5%. No obstante, esta prevalencia aumenta cuando se investiga a celiacos donde la TA se presenta entre el 5-20%. Lo que sugiere realizar la serología de EC en todos aquellos pacientes con enfermedad tiroidea autoinmune. También estudiar la función tiroidea y determinación de anticuerpos antiperoxidasa tiroidea (TPO) y anti-tiroglobulina en todos los pacientes con EC, ya que con la DLG disminuyen los títulos de Ac Anti-TPO. (24)
Personas en riesgo de padecer la enfermedad.
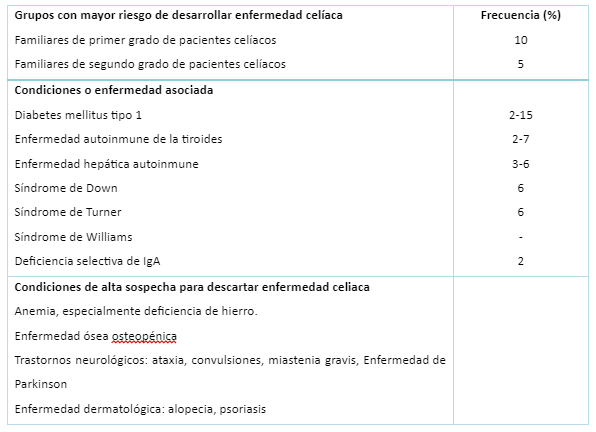
Existe grupo de persona que están en riesgo de desarrollar EC, los cuales deben ser seguidos en el tiempo y debemos conocer que se ha establecido que tienen un riesgo aumentado. Entre ellos los familiares de primer y segundo grado de pacientes celíacos, se estima una prevalencia de 10% y 5% respectivamente. (5) Es prudente aclarar que se consideran familiares de primer grado, padres, hermanos, hijos siendo el riesgo en una posibilidad en 10; para los familiares de segundo grado: tíos, primos, sobrinos con un riesgo de una posibilidad en 39 y para los hermanos gemelos es una posibilidad en dos.
Se ha establecido también como grupo de personas con patologías asociadas como Síndrome de Down, DM tipo 1, deficiencia selectiva de inmunoglobulina A (IgA), tiroiditis autoinmune, Enfermedad hepática autoinmune, Síndrome de Turner y Síndrome de Williams, en la tabla 2. Existen otras patologías donde se ha mencionado el papel del gluten como condición contribuyente como la artritis reumatoidea juvenil, psoriasis, lupus eritematoso sistémico, fibrosis quística, Síndrome de Sjögren, entre otras. (5,25-27)
CONCLUSIONES
La EC tiene múltiples presentaciones clínicas, con síntomas intestinales y extraintestinales, conocerlos nos acerca al diagnóstico. Hay que considerar que existe personas asintomáticas y grupos de riesgo. Sin embargo, se requiere una alta sospecha y corroborar con la solicitud de la serología especifica anticuerpos anti-transglutaminasa tipo IgA, al ser positivos se debe solicitar una segunda muestra con anti-endomisio IgA, dependiendo de los resultados, realizar biopsia intestinal, la cual debe reportar alteraciones histológicas en la biopsia e indicar dieta libre de gluten. Solo en casos dudosos la solicitud del estudio genético.
REFERENCIAS BIBLIOGRÁFICAS
1- Husby S, Koletzko S, Korponay I, Mearin M, Phillips A, y col. ESPGHAN Working Group on Coeliac Disease Diagnosis, on behalf of the ESPGHAN Gastroenterology Committee. European Society of Paediatric Gastroenterology and Nutrition guidelines for the diagnosis for coeliac disease in children and adolescents. An evidence-based approach. J Pediatr Gastroenterol Nutr. 2012;54:136-160.
2- Singh P, Arora A, Strand T, Leffler D, Catassi C, y col. Global Prevalence of Celiac Disease: Systematic Review and Meta-analysis. Clin Gastroenterol Hepatol 2018;16:823–836.e2.
3- Gujral N, Freeman H, Thomson A. Celiac disease: Prevalence, diagnosis, pathogenesis and treatment. World J Gastroenterol 2012; 18(42): 6036-6059.
4- Volta U, Caio G, Stanghellini V, De Giorgio R. The changing clinical profile of celiac disease: a 15-year experience (1998-2012) in an Italian referral center. BMC Gastroenterol 2014;14:194.
5- Sahin Y. Celiac disease in children: A review of the literature. World J Clin Pediatr 2021; 10(4): 53-71.
6- Van Kalleveen M, de Meij T, Plöötz F. Clinical spectrum of paediatric coeliac disease: a 10-year single-centre experience. Eur JPediatr 2018;177:593–602.
7- Popp A, Makki M. Gluten-Induced Extra-Intestinal Manifestations in Potential Celiac Disease – Celiac Trait. Nutrients 2019 ;11 :320-326.
8- Reilly N, Aguilar K, Hassid B, Cheng J, Defelice A, Kazlow P, y col. Celiac disease in normal-weight and overweight children: clinical features and growth outcomes following a gluten-free diet. J Pediatr Gastroenterol Nutr 2011;53:528–531.
9- Therrien A, Ciaram K, Silvester J. Celiac Disease: Extraintestinal Manifestations and Associated Conditions. J Clin Gastroenterol 2020; 54 (1): 8-21.
10- Caio G, Volta U, Sapone A, Leffler D, De Giorgio R, Catassi C, Fasano A. Celiac disease: a comprehensive current review. BMC Med 2019;17(1):142.
11- Panezai M, Ullah A, Ballur K, Gilstrap L, Khan J, y col. Frequency of Celiac Disease in Patients With Chronic Diarrhea. Cureus 2021;13(12):e20495.
12- Horton R, Hagen C, Snyder M. Pediatric Celiac Disease: A Review of Diagnostic Testing and Guideline Recommendations. The Journal of Applied Laboratory Medicine 2022; 7(1):294–304.
13- Ludvigsson J, Leffler D, Bai J, Biagi F, Fasano A, Green H, y col. The Oslo definitions for coeliac disease and related terms. Gut 2013; 62: 43-52.
14- Durazzo, M, Ferro A, Brascugli I, Mattivi S, Fagoonee S, y col. Extra-Intestinal Manifestations of Celiac Disease: What Should We Know in 2022? J Clin Med 2022;11:258..
15- Rispo A, Imperatore N, Guarino M, Tortora R, Alisi A, Cossiga V, Testa A, Ricciolino S, y col. Metabolic-associated fatty liver disease (MAFLD) in coeliac diseaseLiver International 2021;41(4):788-798.
16- Nardecchia S, Auricchio R, Discepolo V and Troncone R. Extra-Intestinal Manifestations of Coeliac Disease in Children: Clinical Features and Mechanisms. Front Pediatr 2019; 7:56.
17- Balaban D, Popp A, Ionita Radu F, Jinga M. Hematologic Manifestations in Celiac Disease A Practical Review. Medicina 2019;55:373-376.
18- Laurikka P, Nurminen S, Kivelä L, Kurppa K. Extraintestinal Manifestations of Celiac Disease: Early Detection for Better Long-Term Outcomes. Nutrients 2018;10(8):1015.
19- Rodrigo L, Betetai V, Alvarez N, Gómez , de Dios A, Palacios L, Santos J. Cutaneous and Mucosal Manifestations Associated with Celiac Disease. Nutrients 2018;10(7):800.
20- Coronel C, Rodríguez A. Neurological Manifestations of the Celiac Disease in Children. OBM Neurobiology 2020; 4(3): 066.
21- Giuffrè M, Gazzin S, Zoratti C, Llido J, Lanza G, y col. Celiac Disease and Neurological Manifestations: From Gluten to Neuroinflammation. Int J Mol Sci 2022;23:15564.
22- Kumar K, Rustogi D. Extraintestinal Manifestations of Celiac Disease in Children. IntechOpen. 2023.
23- Flores G, Islam H, Puttagunta S, Islam R, Kundu S, Jha S, Rivera A, Sange I. Association Between Type 1 Diabetes Mellitus and Celiac Disease: Autoimmune Disorders With a Shared Genetic Background. Cureus 2022;14(3):e22912.
24- Ashok T, Patni N, Fatima M, Lamis A, Siddiqui S. Celiac Disease and Autoimmune Thyroid Disease: The Two Peas in a Pod. Cureus 2022;14(6):e26243.
25- Bai J, Ciacci C, Corazza G, Schuppan D, Farthing M, y col. Celiac Disease 2016 World Gastroenterology Organisation Guidelines. J Clin Gastroenterol 2013;47(2):121-126.
26- Méndez D, Arriola M, Gonzáles A, Montenegro C, Olano C. Prevalencia y características de la deficiencia selectiva de IgA en pacientes celíacos. Rev Gastroenterol Peru. 2021;41(1):11-15
27- Soltani Z, Baghdad A, Nejadhosseinian M, Faezi S, Shahbazkhani B, y col. Celiac disease in patients with systemic lupus erythematosus. Reumatologia 2021; 59(2): 85–89.
Figura 1. Manifestaciones extradigestivas comunes para cualquier grupo de edad
Tabla 1. Distribución de las manifestaciones clínicas según afección intestinal o extraintestinal y fenotipo clásico y no clásico.
Tabla 2. Personas en riesgo de desarrollar enfermedad celiaca y condiciones asociadas.